About PDCPDCについて
PDCとは
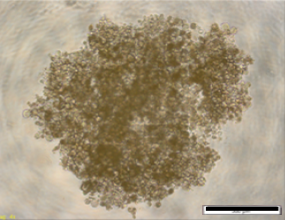
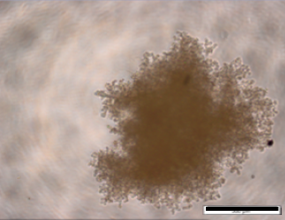
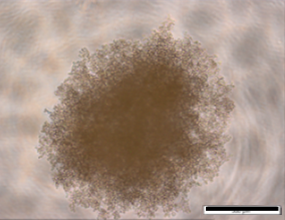
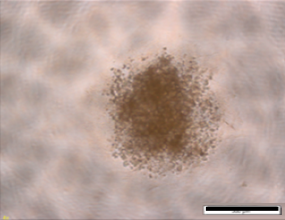
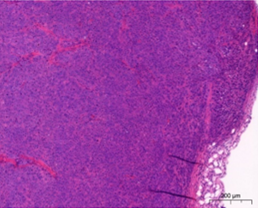
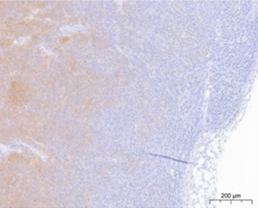
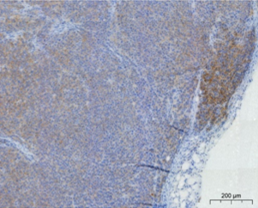
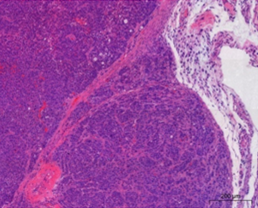
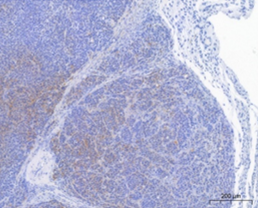
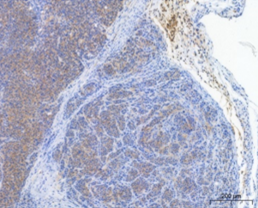
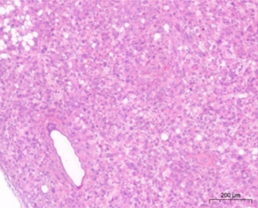
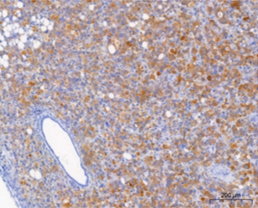
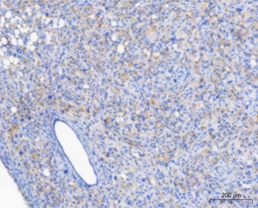
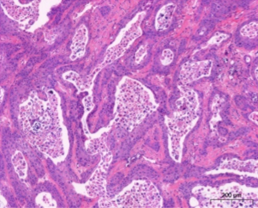
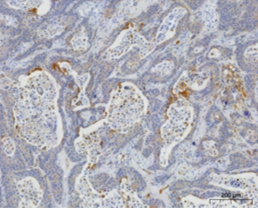
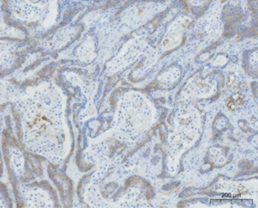
国立がん研究センターが樹立したPDCは、胃がん、膵がんの腹膜播種により腹水が貯留した患者さんの腹水に含まれる細胞から樹立した細胞株です。低継代数で保存しており、腫瘍細胞を含む不均一な細胞集団を維持しています。培養細胞株よりも患者さんのがん組織中のがん細胞に近い状態を維持していることから、抗がん剤の薬効の確認に有用です。

PDCの特徴
- 患者から採取したがん細胞を3回または5回継代し,株化したもの
- 100継代前後まで使用予定
- 全エクソーム解析,マイクロアレイ(Affymetrix U133 Plus 2.0)を実施
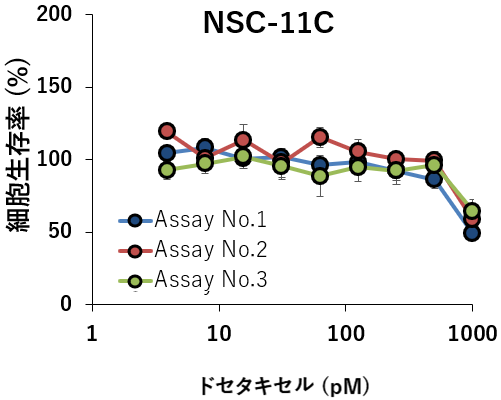
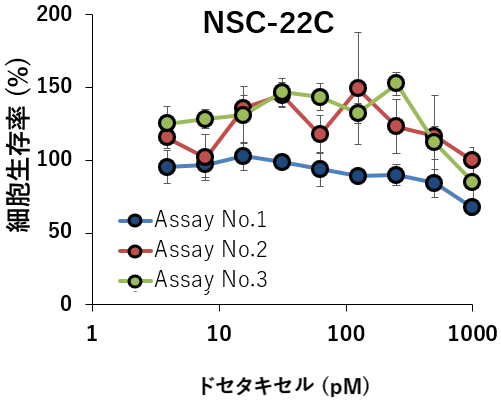
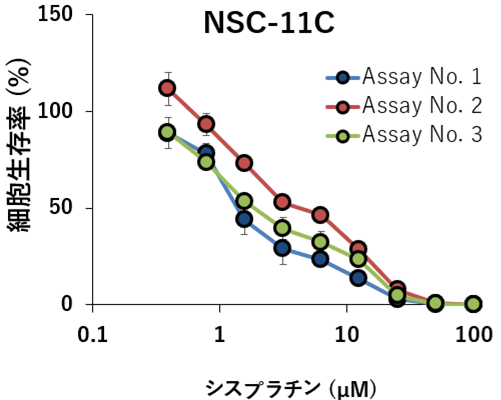
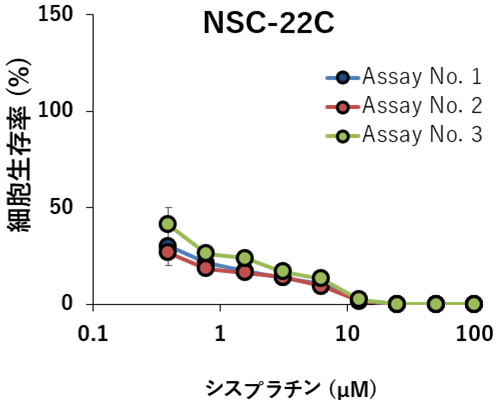
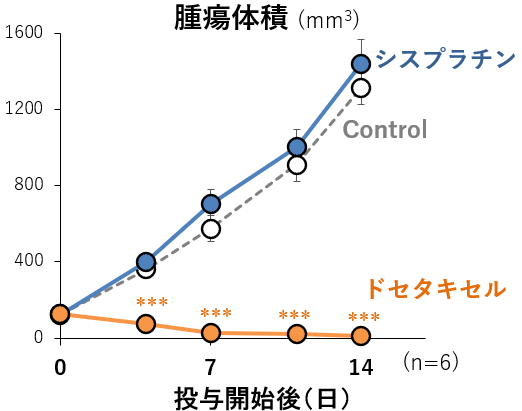
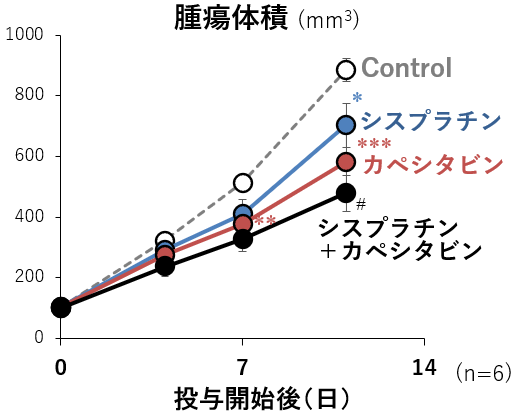
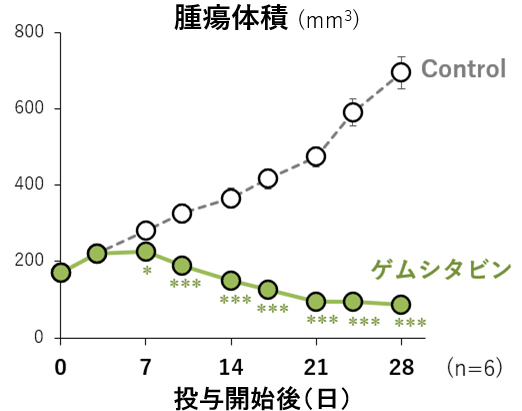
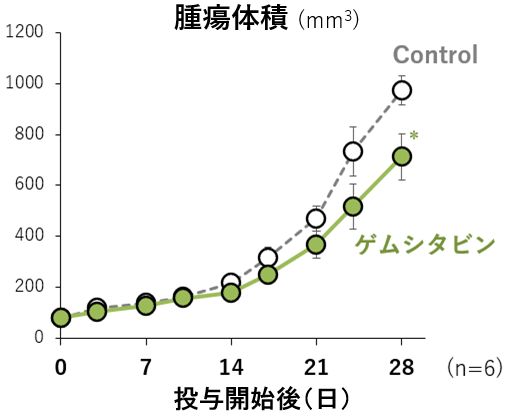
- 当社と国立がん研究センターで,in vitro(2D培養)での薬効評価を実施
( シスプラチン, ドセタキセル,ゲムシタビン等を使用)
胃がん患者の腹水由来PDC:45株
スキルス胃がんに代表される予後不良のびまん型胃がんの細胞株
参考論文:
Tanaka Y, Chiwaki F, .., Sasaki H, Mano H. Multi-omic profiling of peritoneal metastasis in gastric cancer identifies molecular subtypes and therapeutic vulnerabilities. Nat. Cancer. 2021 Aug. doi.org/10.1038/s43018-021-00240-6.
Komatsu M, .., Sasaki H. ARHGAP–RhoA signaling provokes homotypic adhesion-triggered cell death of metastasized diffuse-type gastric cancer. Oncogene. 2022 Sept 20. doi.org/10.1038/s41388-022-02469-6.
膵臓がん患者の腹水由来PDC:38株
腺がん36株、扁平上皮がん1株、腺扁平上皮がん1株
参考文献:
佐々木博己編著「患者由来がんモデルを用いたがん研究実践ガイド」、羊土社、2019.